Siamo ormai arrivati a fronte dell’entrata in vigore della nuova direttiva Dispositivi Medici 2017/745 prevista per Maggio 2021.
Il Centro Studi dell’Associazione Italiana degli Ingegneri Clinici ha deciso di stilare un documento con le linee guida per l’utilizzo delle tecnologie di Additive Manufacturing all’interno di strutture ospedaliere. Negli ultimi anni il supporto delle tecnologie additive all’interno del settore sanitario si è rilevato preponderante come metodologia di fabbricazione di dispositivi su misura e performanti, mettendo al centro dell’attenzione l’importanza di una terapia personalizzata sul paziente.
Inoltre, l’avanzamento dello sviluppo delle tecnologie 3D nei settori industriali sta superando la funzione iniziale che ne vedeva il vantaggio principale nella versatilità e velocità con cui si integra nella fase di prototipazione fino alla necessità di introdurlo in una vera e propria tecnologia per la produzione in serie.
Questo documento è stato redatto principalmente per fare chiarezza e aiutare gli esperti nell’ambito, dalle strutture ospedaliere alle aziende, a classificare e identificare i diversi usi delle tecnologie di Additive Manufacturing e della loro integrazione nell’ambiente sanitario.
Il focus principale del documento riguarda la progettazione e produzione di dispositivi medici stampati in 3D seguendo un flusso di lavoro preciso in cui sono state individuate le figure cliniche competenti a gestire le varie fasi del processo dall’acquisizione dei dati fino alla progettazione. All’interno vengono classificate diverse tipologie di applicazioni cliniche con la AM in base alla finalità di utilizzo identificando gli aspetti regolatori tra un dispositivo medico e un dispositivo medico su misura.
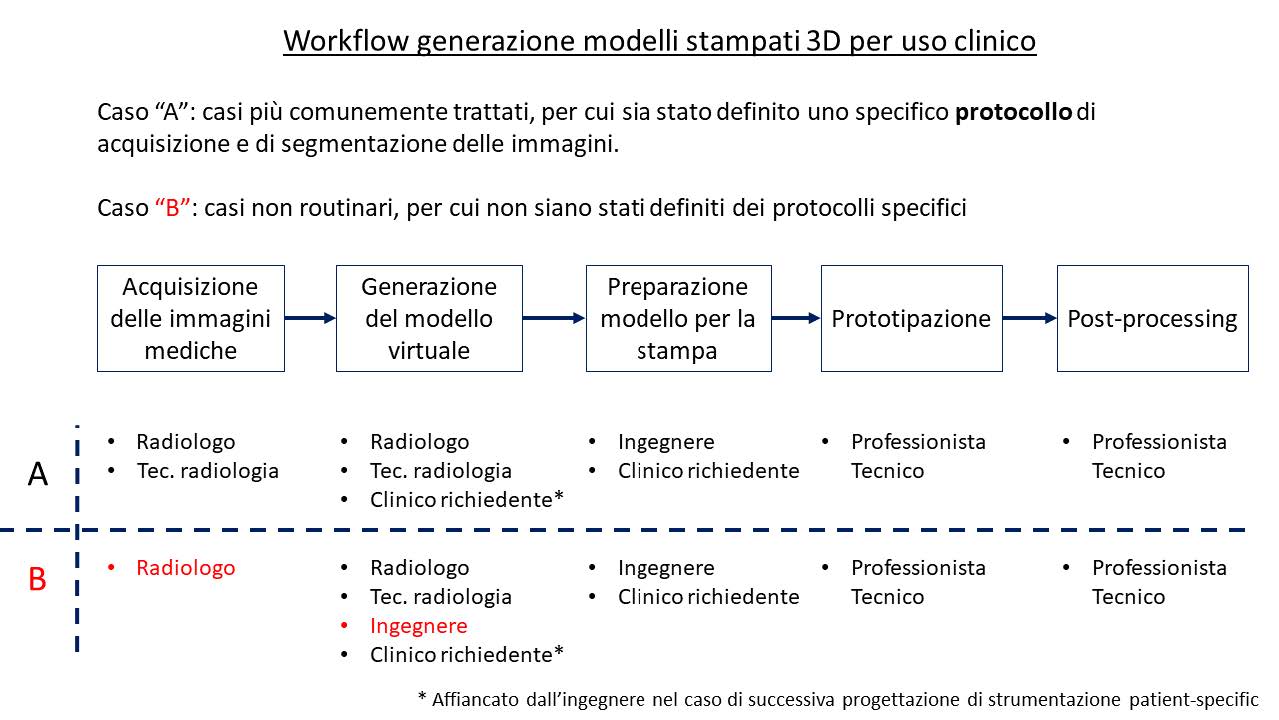
Workflow di generazione di modelli stampati 3D per uso clinico. Indicazione delle figure coinvolte nel caso in cui sia definito uno specifico protocollo di acquisizione (Caso “A”) o nel caso in cui non sia definito uno specifico protocollo (Caso “B”).
Inoltre per ogni iter di progettazione e produzione a seconda che il fabbricante identificato sia una struttura sanitaria o privata vengono individuate le linee da seguire citando direttamente le nuove direttive Europee Dispositivi Medici e Dispositivi Medici Impiantabili In Vitro rispettivamente 2017/745 e 2017/746, partendo dalla distinzione tra dispositivo medico prodotto in serie e dispositivo medico su misura.
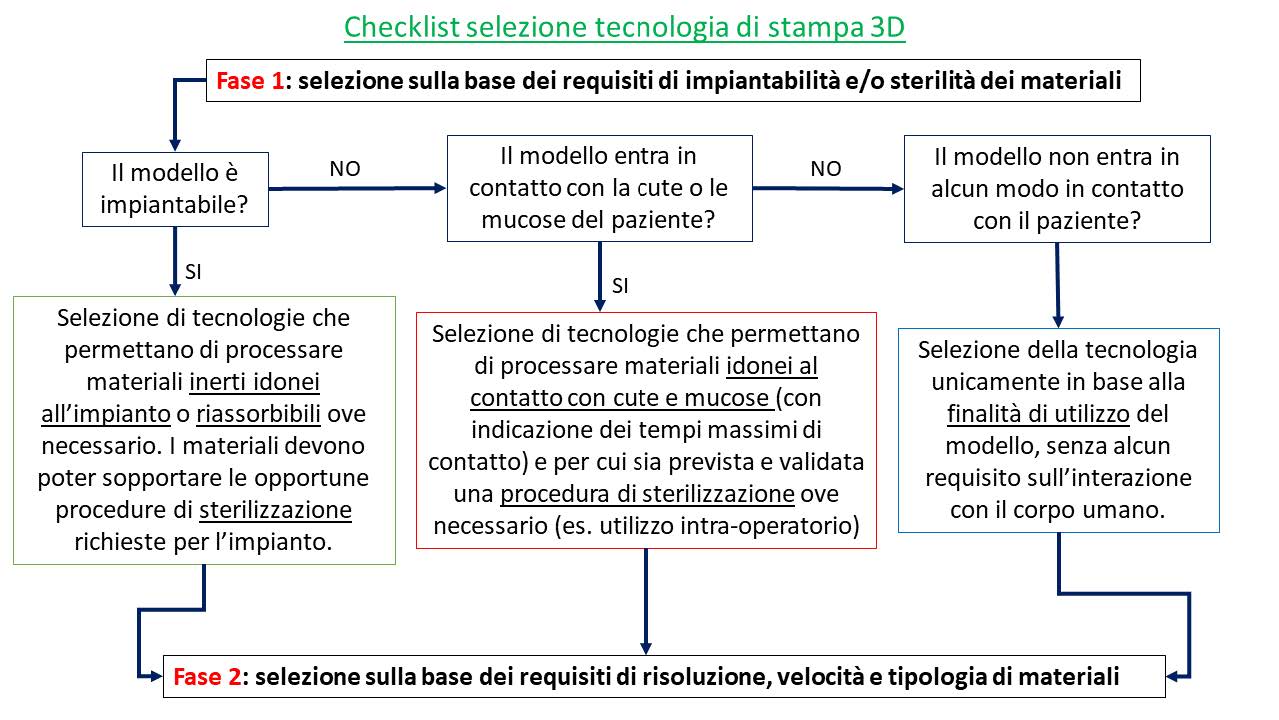
Checklist di selezione della tecnologia di stampa 3D da utilizzare per la produzione. Processo in due fasi: 1) selezione sulla base di requisiti di impiantabilità e/o sterilità, e 2) selezione sulla base di requisiti di risoluzione, velocità e tipologia di materiali disponibili.
Cos’è un Dispositivo Medico?
«Dispositivo medico»: qualunque strumento, apparecchio, apparecchiatura, software, impianto, reagente, materiale o altro articolo, destinato dal fabbricante a essere impiegato sull'uomo, da solo o in combinazione, per una o più delle seguenti destinazioni d'uso mediche specifiche:
- diagnosi, prevenzione, monitoraggio, previsione, prognosi, trattamento o attenuazione di malattie
- diagnosi, monitoraggio, trattamento, attenuazione o compensazione di una lesione o di una disabilità
- studio, sostituzione o modifica dell'anatomia oppure di un processo o stato fisiologico o patologico
- fornire informazioni attraverso l'esame in vitro di campioni provenienti dal corpo umano, inclusi sangue e tessuti donati, e che non esercita nel o sul corpo umano l'azione principale cui è destinato mediante mezzi farmacologici, immunologici o metabolici, ma la cui funzione può essere coadiuvata da tali mezzi.
Si considerano dispositivi medici anche i seguenti prodotti:
- dispositivi per il controllo del concepimento o il supporto al concepimento
- i prodotti specificamente destinati alla pulizia, disinfezione o sterilizzazione dei dispositivi di cui all'articolo 1, paragrafo 4, e di quelli di cui al primo comma del presente punto
1 Regolamento 2017/745 articolo 2 punto 1
Cos’è un Dispositivo su Misura?
«Dispositivo su misura»: qualsiasi dispositivo fabbricato appositamente sulla base di una prescrizione scritta di qualsiasi persona autorizzata dal diritto nazionale in virtù della sua qualifica professionale, che indichi, sotto la responsabilità di tale persona, le caratteristiche specifiche di progettazione, e che è destinato a essere utilizzato solo per un determinato paziente esclusivamente al fine di rispondere alle sue condizioni ed esigenze individuali. I dispositivi fabbricati in serie che devono essere adattati per soddisfare le esigenze specifiche di un utilizzatore professionale e i dispositivi che sono fabbricati in serie mediante processi di fabbricazione industriale conformemente alle prescrizioni scritte di qualsiasi persona autorizzata non sono tuttavia considerati dispositivi su misura;
2 Regolamento 2017/745 articolo 2 punto 3
Le differenze tra le due tipologie di dispositivo determinano un iter di progettazione, produzione e certificazione del prodotto finito che prevede degli obblighi diversi in relazione alle normative.
Sulla base delle principali applicazioni mediche e cliniche in cui è stata declinata la stampa 3D negli ultimi anni, vengono quindi distinte in particolare alcune classi di modelli e dispositivi:
- Modelli anatomici per pianificazione chirurgica e training chirurgico (cosiddetti phantom), realizzati principalmente per guidare il medico nella pianificazione chirurgica all’intervento.
Sono stati distinti in particolar modo tra quelli didattici che non ricadono nella definizione di dispositivo medico e quelli appositamente fabbricati per la preparazione del chirurgo all’intervento, i quali una volta sottoposti al vaglio sono stati fatti ricadere nelle regole più stringenti come dispositivi medici, nonostante non vengano a diretto contatto con il paziente ma ne sono coinvolti nel processo di cura. In questo caso è necessario verificare che il software utilizzato nella ricostruzione e le stampanti 3D siano regolamentati.
- Protesi, ortesi e ausili su misura,dispositivi a contatto diretto con la cute e i tessuti per un periodo di tempo definito
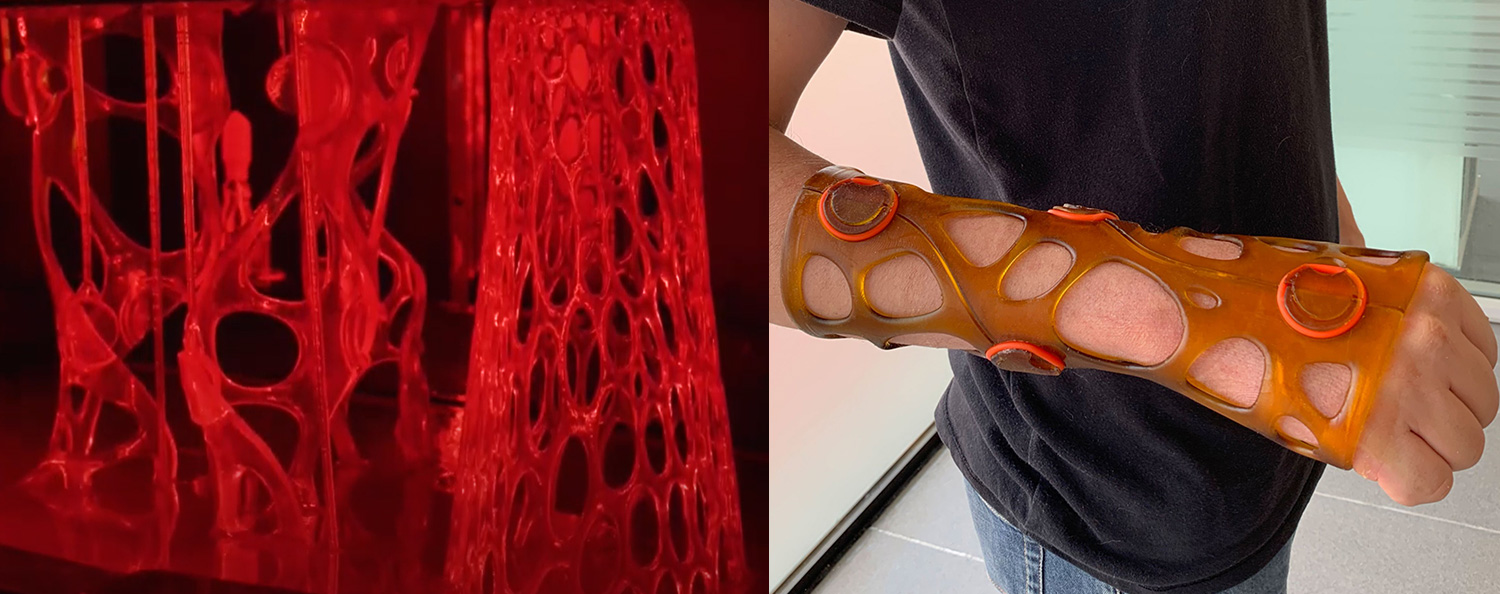 Fonte: Photocentric, caso di studio Xkelet
Fonte: Photocentric, caso di studio Xkelet - Strumentazione chirurgica, strumenti chirurgici progettati esclusivamente sull’anatomia del paziente per guidare l'operazione nel corso dell'intervento, un esempio sono le dime di taglio utilizzate in ambito maxillo-facciale e ortopedico.
Le guide chirurgiche e di taglio ricadono invece nella condizione di dispositivi medici su misura perché progettati ad hoc sul paziente e applicati direttamente a contatto, quindi è necessario siano sottoposti a pratiche di sterilizzazione.
- Dispositivi protesici impiantabili o indossabili, dispositivi impiantati nel corpo permanentemente. Tipici sono quelli in materiale metallico, studiati nel design per garantire le performance del dispositivo dal punto di vista dell'osteointegrazione.
Devono rispondere a specifici requisiti perché progettati appositamente per il paziente con materiali altamente compatibili per l’inserimento a lungo termine. - Bioprinting e scaffolding, processi che si avvalgono delle tecnologie AM per la deposizione di materiale vivente e non vivente, in particolar modo nell’ambito dell’ingegneria rigenerativa e dei tessuti
- Dispositivi prodotti in serie, fabbricati con tecnologia additiva per l’efficienza di produzione maggiore. Ricadono nella classe dispositivi medici seguendo i requisiti specifici.

Per aiutare chi legge il documento a comprendere al meglio i requisiti richiesti al fine di certificare il prodotto, sono stati esemplificati i doveri legislativi in merito alla normativa utilizzando tre semplici parole chiave: sicurezza, beneficio e qualità, per associare direttamente le norme e gli standard ISO a cui far riferimento.
Quando si parla di sicurezza ci si riferisce in particolar modo allo standard ISO 10993 che regola la biocompatibilità dei materiali e gli standard inerenti ai cicli di sterilizzazione e test da carico.
Lo standard ISO 10993 regola in particolar modo la valutazione biologica dei dispositivi medici che prevedono il contatto diretto con il paziente (mucose, tessuti, vasi sanguigni, cute…). In questo senso è più utile per il fabbricante o la struttura ospedaliera dotarsi dei materiali già sottoposti e certificati rispetto a tali test dal produttore.
Abbinato a questo standard c’è quello ISO 14971 riferito alla gestione del rischio che assiste il fabbricante di dispositivi medici nell’identificazione delle situazioni di pericolo e valutazione delle misure di controllo da intraprendere.
Nell’identificazione di beneficio invece si intende dimostrare che vi è una relazione statisticamente significativa tra l’adeguata performance tecnica del dispositivo e l’effetto beneficio clinico al paziente.
La realizzazione di un sistema di qualità adeguato deve rispondere invece alle linee guida di buone pratiche secondo la norma ISO 13485:2016. Seguendo questa norma ci sono tutte le indicazioni per la creazione e la gestione delle procedure destinate a ricreare un'organizzazione di produzione biomedicale controllata e ripetibile.
Un aspetto interessante all’interno del documento riguarda una particolare deroga per le istituzioni sanitarie. All’interno del nuovo regolamento 2017/745 è presente l’art. 5 che riguarda una disciplina specifica circa le istituzioni sanitarie che vogliano produrre dispositivi medici al loro interno utilizzati sui pazienti della struttura.
Il testo cita fedelmente:
“Le istituzioni sanitarie dovrebbero avere la possibilità di fabbricare, modificare e utilizzare internamente dispositivi, rispondendo in tal modo, su scala non industriale, alle esigenze specifiche dei gruppi di pazienti destinatari che non possono essere soddisfatte con risultati del livello adeguato da un dispositivo equivalente disponibile sul mercato.
In tale contesto, è opportuno prevedere che talune disposizioni del presente regolamento non siano applicate per quanto riguarda i dispositivi medici fabbricati e utilizzati esclusivamente nell'ambito di istituzioni sanitarie, compresi ospedali e istituzioni, quali laboratori e istituti di salute pubblica che sostengono il sistema sanitario e/o rispondono alle esigenze dei pazienti, ma che non si occupano direttamente del trattamento o della cura dei pazienti, dal momento che gli obiettivi del presente regolamento sarebbero comunque soddisfatti in modo adeguato.
È opportuno rilevare che il concetto di «istituzione sanitaria» non comprende le aziende i cui obiettivi principali dichiarati sono collegati alla salute e a stili di vita sani, per esempio palestre, terme, centri benessere e centri fitness. Di conseguenza, la deroga applicabile alle istituzioni sanitarie non si applica a tali aziende.”
Vengono quindi definiti i termini di identificazione di una istituzione sanitaria e gli obblighi di intervento rispetto alla produzione di dispositivi medici unicamente per pazienti interni e non a fini di distribuzione terzi, l’identificazione della figura giuridica di riferimento e di tutta la documentazione richiesta.
La realizzazione di questo documento ha messo in evidenza l’importanza che si sta riversando su queste tecnologie all’interno della sanità, facilitando gli operatori sanitari e le figure interessate nella gestione e nell’introduzione di un flusso di lavoro digitale e innovativo.